|
||||||||
Хімічні властивості бензену: горіння, реакції заміщення, приєднання відношення до розчину калій перманганату
Хімічні властивості бензену: горіння, реакції заміщення, приєднання відношення до розчину калій перманганату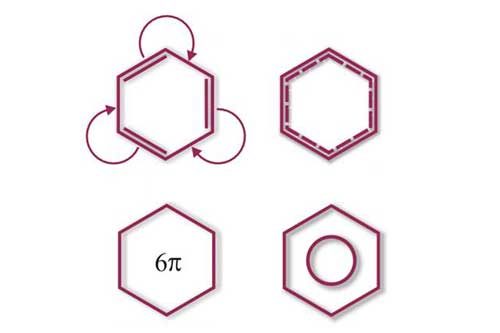 Бензол горить кіптявим полум’ям, утворюючи вуглекислий газ і воду. Особливий вид хімічного зв’язку в молекулі бензолу (ароматичний) обумовлює його стійкість проти дії окисників. Бензол не знебарвлює фіолетовий розчин калій перманганату. Бензол горить кіптявим полум’ям, утворюючи вуглекислий газ і воду. Особливий вид хімічного зв’язку в молекулі бензолу (ароматичний) обумовлює його стійкість проти дії окисників. Бензол не знебарвлює фіолетовий розчин калій перманганату.Як і насичені вуглеводні бензол вступає в реакції заміщення. Це реакції галогенування і нітрування. ЧИТАЙТЕ ТАКОЖ: Застосування бензену. Поняття про хімічні засоби захисту рослин Реакції заміщення за участю бензолу відбуваються легше, ніж у насичених вуглеводнів. Так, при взаємодії бензолу з бромом при наявності каталізатора FeBr3 відбувається заміщення атома Гідрогену атомом Брому і утворюється бромобензол C6H5Br і бромоводень HBr. C6H6 + Br2 C5H5Br + HBr Продуктами іншої реакції заміщення - реакції нітрування - є нітробензол C6H5NO2 і вода. C6H6 + HNO3 → C6H5NO2 + H2O Як і ненасичені вуглеводні, бензол вступає в реакції приєднання. Це реакції хлорування при ультрафіолетовому освітленні C6H6 + 3Cl2 C6H6Cl6 та реакція гідрування C6H6 + 3H2 → C6H12 Реакції приєднання до бензолу проходять значно важче, ніж у ненасичених вуглеводнів. Щоб вони відбулися, потрібні особливі умови: підвищення температури і тиску, підбір каталізатора, світлове опромінювання та інше. Так, з каталізатором - нікелем чи платиною - бензол приєднує водень, утворюючи циклогексан C6HC12. При ультрафіолетовому опромінювання бензол приєднує хлор, утворюючи гексахлорциклогексан C6H6Cl6. ЧИТАЙТЕ ТАКОЖ: Взаємозв’язок насичених, ненасичених і ароматичних вуглеводнів Добувають бензол у лабораторії тримеризацією ацетилену, дегідруванням циклогексану та гексану. У великих кількостях бензол добувають із нафти і кам’яного вугілля під час їх переробки. | ||
|
Схожі матеріали:
| ||
| Всього коментарів: 0 | |
|
ЗАРАЗ ЧИТАЮТЬ
|
|
|
 |  |
 |  |
 |  |
 |  |
 |  |













