|
|||||||||
✔️ Освіта
У розділі матеріалів: 313
Показано матеріалів: 251-260
Показано матеріалів: 251-260
|
|
Англійська мова. Універсальне видання - підготовка до ЗНО та ДПА. Фонетика. Вплив приголосних на читання деяких голосних Буквосполучення о + ld читається [ould]: cold [kould]. Буквосполучення о + ld читається [ould]: cold [kould].Буква і у сполученні з ld, nd, gh читається [ai]: child [t∫aild], kind [kaind], high [hai]. Примітка: В сучасній англійській мові сполучення gh не читається у жодному слові. Буква а читається [α:] перед буквосполученнями ss, st, sk, sp: pass [pα:s], past [pα:st], ask [α:sk], grasp [grα:sp]. Буква a читається [α:] також перед буквосполученнями nt, nсе, nch: plant [plα:nt], dance [dα:ns], branch [brα:nt∫]. |
Англійська мова. Універсальне видання - підготовка до ЗНО та ДПА. Фонетика. Правила читання приголосних В англійській мові є глухі і дзвінкі приголосні. В англійській мові є глухі і дзвінкі приголосні.Наступні приголосні читаються глухо, тобто без голосу: f [f], t [t], р [р], к [k], h [h], s [s]. Буква x передає сполучення звуків [ks]. Такі приголосні читаються дзвінко, тобто з голосом: d [d], b [b], g [g], z [z], n [n], m [m], l [l], r [r]. В англійській мові дзвінкі приголосні у кінці слова не можна оглушувати. |
|
Англійська мова. Універсальне видання - підготовка до ЗНО та ДПА. Фонетика. Правила читання голосних
Англійська мова. Універсальне видання - підготовка до ЗНО та ДПА. Фонетика. Правила читання голосних В англійській мові голосні можуть читатися у словах по-різному, залежно від їхнього положення у слові, а також від того, які букви стоять перед ними або позаду них. В англійській мові голосні можуть читатися у словах по-різному, залежно від їхнього положення у слові, а також від того, які букви стоять перед ними або позаду них.1) Якщо голосна знаходиться у відкритому складі (І тип складу), вона читається як в алфавіті. |
Нітроген і Фосфор, їх місце в Періодичній системі будови атомів. Алотропні модифікації Фосфору. Азот і Фосфор як прості речовини: будова молекул, поширення в природі. Фізичні властивості азоту і фосфору. Хімічні властивості азоту та фосфору: взаємодія з металами, воднем, киснем. Застосування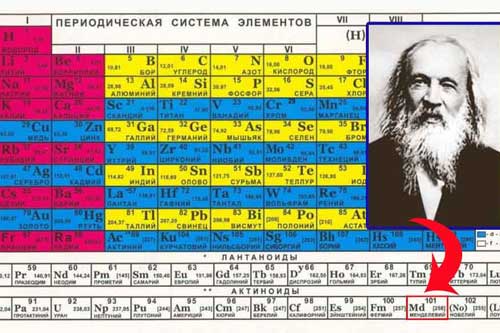 Нітроген і Фосфор у Періодичній системі хімічних елементів знаходяться в головній підгрупі п’ятої групи. На зовнішньому енергетичному шарі обидва елемента містять по 5 електронів у стані s2p3. Тому найвищий ступінь окиснення цих елементів дорівнює +5, найнижчий - –3. Нітроген і Фосфор у Періодичній системі хімічних елементів знаходяться в головній підгрупі п’ятої групи. На зовнішньому енергетичному шарі обидва елемента містять по 5 електронів у стані s2p3. Тому найвищий ступінь окиснення цих елементів дорівнює +5, найнижчий - –3.Відмінність полягає у тому, що в атомі Фосфору на зовнішньому електронному шарі є вільні d-орбіталі. Це дає можливість йому приходити у збуджений стан. |
Амоніак: будова молекули, одержання в лабораторії. Фізичні та хімічні властивості амоніаку. Взаємодія з киснем, водою, кислотами. Застосування амоніаку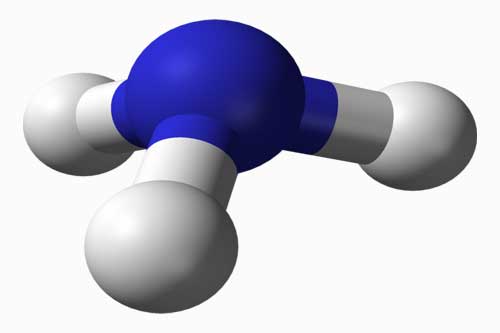 Молекулярна формула аміаку NH3. У молекулі аміаку атом Нітрогену пов’язаний із трьома атомами Гідрогену ковалентним полярним зв’язком. Густина його зміщена у бік атома Нітрогену, як більш електронегативного. І тому молекула аміаку являє собою диполь. Молекулярна формула аміаку NH3. У молекулі аміаку атом Нітрогену пов’язаний із трьома атомами Гідрогену ковалентним полярним зв’язком. Густина його зміщена у бік атома Нітрогену, як більш електронегативного. І тому молекула аміаку являє собою диполь.У лабораторії аміак добувають слабким нагріванням суміші амоній хлориду NH4Cl з гашеним вапном Ca(OH)2. |
Солі амонію. Фізичні властивості солей амонію. Хімічні властивості: взаємодія з лугами, солями, розкладання під час нагрівання. Якісна реакція на йони амонію, одержання солей амонію в лабораторії Солі амонію складаються з катіона амонію NH4+ та аніона кислоти. За будовою вони аналогічні солям лужних металів. Солі амонію складаються з катіона амонію NH4+ та аніона кислоти. За будовою вони аналогічні солям лужних металів.За фізичними властивостями солі амонію - це тверді кристалічні речовини. Добре розчиняються у воді. Солі амонію виявляють типові для всіх солей хімічні властивості і деякі специфічні. Як і всі розчинні солі, солі амонію у водному розчині добре дисоціюють на йони, взаємодіють із лугами, сильними кислотами, іншими солями. |
Промисловий синтез амоніаку: вибір оптимальних умов синтезу, будова й робота колони синтезу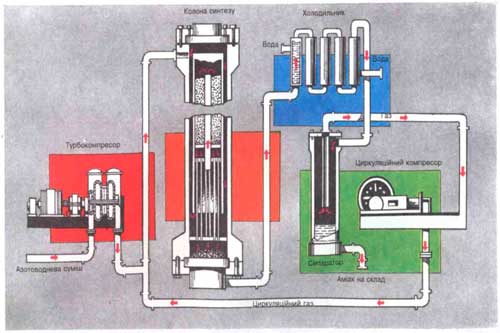 Основним способом добування аміаку в промисловості є синтез його з азоту і водню: N2 + 3H2 ® 2NH3. Ця реакція є оборотною, екзотермічною та відбувається лише при наявності каталізатора. Основним способом добування аміаку в промисловості є синтез його з азоту і водню: N2 + 3H2 ® 2NH3. Ця реакція є оборотною, екзотермічною та відбувається лише при наявності каталізатора.Основним завданням будь-якого виробництва є не просто добути задану речовину, а добути її найбільш економічним способом. А для цього необхідно підібрати оптимальні умови синтезу, тобто такі, за яких вихід продукту буде найбільшим і процес здійснюватиметься з великою швидкістю. |
Нітроген(II) і нітроген(IV) оксиди. Фосфор (V) оксид. Їх фізичні та хімічні властивості. Застосування Нітроген з Оксигеном утворює шість оксидів, у яких він виявляє ступені окиснення від +1 до +5, це оксиди складом відповідно N2O, NO, N2O3, NO2, N2O4. З них при безпосередньому сполученні азоту з киснем утворюється лиш нітроген(II) оксид NO. Нітроген з Оксигеном утворює шість оксидів, у яких він виявляє ступені окиснення від +1 до +5, це оксиди складом відповідно N2O, NO, N2O3, NO2, N2O4. З них при безпосередньому сполученні азоту з киснем утворюється лиш нітроген(II) оксид NO. Інші оксиди добувають непрямими способами. З оксидів азоту два оксиди є несолетворними. Це нітроген один оксид N2O і нітроген два оксид NO. Усі інші оксиди - солетворні. Усі оксиди Нітрогену дуже отруйні, за винятком N2O. Розглянемо нітроген (II) оксид і нітроген(IV) оксид. |
Нітратна й ортофосфатна кислоти. Їх фізичні та хімічні властивості Молекулярна формула нітратної кислоти HNO3. Це безбарвна рідина з їдким запахом. На повітрі «димить». Дуже добре розчиняється у воді, змішуючись з нею у будь-яких співвідношеннях. Кипить при температурі 86 °С. Молекулярна формула нітратної кислоти HNO3. Це безбарвна рідина з їдким запахом. На повітрі «димить». Дуже добре розчиняється у воді, змішуючись з нею у будь-яких співвідношеннях. Кипить при температурі 86 °С.Нітратна кислота - сильний електроліт, у водному розчині практично повністю дисоціює на йони. Розведена нітратна кислота має хімічні властивості, типові для всіх кислот. Вона реагує з оксидами металів, основами, солями більш слабких кислот. Концентрована нітратна кислота - сильний окисник. Вона активно реагує з неметалами, розкладається при нагріванні і під впливом світла. |
Особливості взаємодії розбавленого і концентрованого розчинів нітратної кислоти з міддю. Застосування нітратної й ортофосфатної кислот Нітратна кислота реагує з металами інакше, ніж інші кислоти. Це пояснюється тим, що вона - сильний окисник. Нітратна кислота окислює майже всі метали. Нітратна кислота реагує з металами інакше, ніж інші кислоти. Це пояснюється тим, що вона - сильний окисник. Нітратна кислота окислює майже всі метали. При цьому слід пам’ятати, що концентрована нітратна кислота не реагує з алюмінієм, залізом, хромом, іридієм, танталом. Вона їх пасивує. Тому її зберігають і перевозять у тарі, виготовленій із цих металів. |
|
ЕНЦИКЛОПЕДІЯ КОРИСНОГО
|